Pengarang:
Lewis Jackson
Tanggal Pembuatan:
12 Boleh 2021
Tanggal Pembaruan:
1 Juli 2024

Isi
Menentukan jumlah neutron dalam atom cukup sederhana, Anda bahkan tidak perlu melakukan eksperimen apa pun. Untuk menghitung jumlah neutron dalam atom atau isotop normal, Anda hanya perlu menyiapkan tabel periodik dan mengikuti petunjuknya.
Langkah
Metode 1 dari 2: Temukan jumlah neutron dalam atom normal
Tentukan posisi unsur pada tabel periodik. Misalnya, kita akan mencari elemen osmium (Os) di baris keenam dari atas.
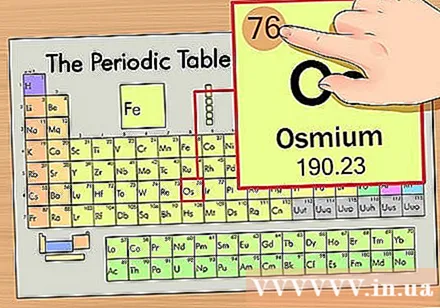
Temukan nomor atom unsur tersebut. Ini adalah angka paling terlihat yang melewati setiap elemen dan berada di atas simbol prima (di papan yang kami gunakan tidak ada angka lain). Nomor atom adalah jumlah proton dalam satu atom unsur itu. Os adalah bilangan 76 yang artinya terdapat 76 proton dalam sebuah atom osmium.- Jumlah proton tidak pernah berubah dalam suatu unsur; itu pada dasarnya adalah karakteristik yang menentukan dari suatu elemen.
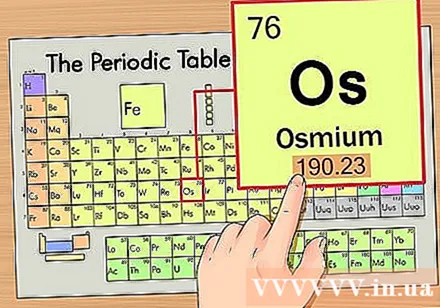
Tentukan berat atom unsur tersebut. Angka ini biasanya ditemukan di bawah simbol prima. Perhatikan bahwa tabel periodik dalam contoh ini hanya memiliki nomor atom dan tidak memiliki berat atom. Tidak semua tabel periodik. Osmium memiliki berat atom 190,23.
Bulatkan berat atom ke bilangan bulat terdekat untuk mendapatkan massa atom. Misalnya, 190,23 akan dibulatkan menjadi 190, sehingga massa atom osmium adalah 190.- Berat atom adalah rata-rata isotop dari unsur kimia yang sama, itulah sebabnya ia biasanya bukan bilangan bulat.
Kurangi nomor atom dari massa atom. Karena sebagian besar massa atom adalah massa proton dan neutron, mengurangkan jumlah proton dari massa atom (yaitu nomor atom) Anda akan menghitung dapatkan jumlah neutron di atom. Angka setelah titik desimal menunjukkan massa elektron yang sangat kecil dalam atom. Dalam contoh ini, kita memiliki: 190 (massa atom) - 76 (jumlah proton) = 114 (jumlah neutron).
Hafalkan resepnya. Untuk mencari jumlah neutron, kita cukup menerapkan rumus berikut: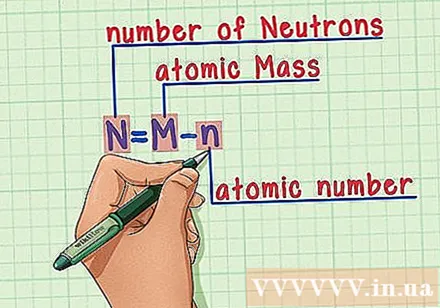
- N = M - n
- N = jumlah neutron
- M = massa atom
- n = nomor atom
- N = M - n
Metode 2 dari 2: Temukan jumlah neutron dalam isotop
Tentukan posisi unsur pada tabel periodik. Mari kita ambil isotop unsur karbon-14 sebagai contoh. Karena bentuk isotop karbon-14 hanyalah karbon (C), carilah karbon pada tabel periodik (baris kedua dari atas).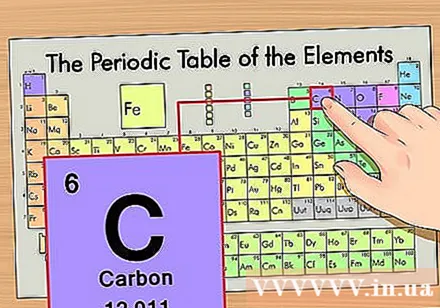
Temukan nomor atom unsur tersebut. Ini adalah angka paling terlihat yang melewati setiap elemen dan berada di atas simbol prima (di papan yang kami gunakan tidak ada angka lain). Nomor atom adalah jumlah proton dalam satu atom unsur itu. C adalah angka 6 yang artinya ada 6 proton dalam satu atom karbon.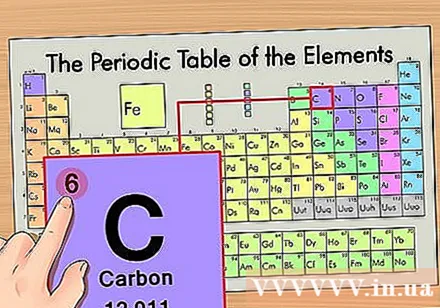
Temukan massa atom. Ini sangat mudah dilakukan dengan isotop karena dinamai menurut massa atom. Misalnya, karbon-14 akan memiliki massa atom 14. Setelah Anda menemukan massa atom isotop, langkah yang tersisa untuk mencari jumlah neutron akan sama dengan langkah pada atom normal.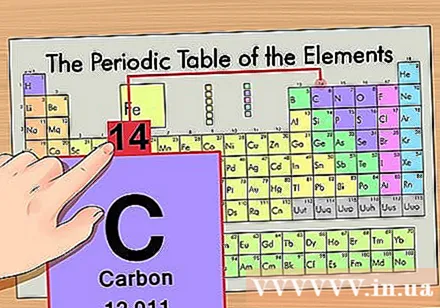
Kurangi nomor atom dari massa atom. Karena sebagian besar massa atom adalah massa proton dan neutron, mengurangkan jumlah proton dari massa atom (yaitu nomor atom) Anda akan menghitung dapatkan jumlah neutron di atom. Angka setelah titik desimal menunjukkan massa elektron yang sangat kecil dalam atom. Dalam contoh ini, kita memiliki: 14 (atom massa) - 6 (jumlah proton) = 8 (jumlah neutron).
Hafalkan resepnya. Untuk mencari jumlah neutron, kami menerapkan rumus berikut: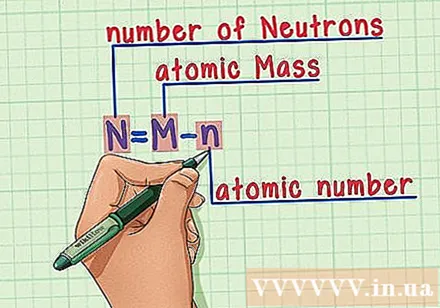
- N = M - n
- N = jumlah neutron
- M = massa atom
- n = nomor atom
- N = M - n
Nasihat
- Massa suatu unsur sebagian besar adalah massa proton dan neutron, sedangkan massa elektron dan unsur lainnya dapat diabaikan (mendekati nol). Karena massa proton kira-kira sama dengan massa neutron, dan nomor atom mewakili jumlah proton, kita hanya perlu mengurangkan jumlah proton dari massa total.
- Jika Anda tidak ingat arti angka-angka pada tabel periodik, ingatlah bahwa tabel periodik biasanya dibangun di atas nomor atom (yaitu jumlah proton), dimulai dari 1 (hidrogen) dan bertambah satu unit dari kiri ke kanan, diakhiri dengan 118 (ununoctium). Karena jumlah proton adalah ciri pengenal setiap atom, ini adalah sifat paling sederhana yang menyusun unsur-unsur. (Misalnya, atom dengan 2 proton selalu helium, seperti atom dengan 79 proton selalu emas.)
Sumber dan Kutipan
- Tabel periodik interaktif