Pengarang:
Monica Porter
Tanggal Pembuatan:
17 Berbaris 2021
Tanggal Pembaruan:
1 Juli 2024

Isi
Konsentrasi molar menunjukkan hubungan antara jumlah mol zat terlarut dan volume larutan. Untuk menghitung molaritas, Anda bisa mulai dengan mol dan volume, massa dan volume, atau mol dan mililiter (ml). Kemudian, dengan variabel di atas, gunakan rumus konsentrasi molar dasar untuk mendapatkan hasil yang benar.
Langkah
Metode 1 dari 4: Hitung Konsentrasi Mol dari Jumlah dan Volume Molar
Penting untuk mengetahui rumus dasar untuk menghitung konsentrasi molar. Konsentrasi molar sama dengan jumlah mol zat terlarut dibagi volume larutan dalam liter. Dari sana, kami memiliki rumus berikut: Konsentrasi molar = jumlah mol zat terlarut / jumlah liter larutan
- Contoh: Berapa konsentrasi molar dari larutan yang mengandung 0,75 mol NaCl dalam 4,2 liter larutan?

Analisis topiknya. Untuk menghitung konsentrasi molar, Anda membutuhkan jumlah mol dan volume larutan dalam liter. Anda tidak perlu menghitung kedua nilai ini karena topik yang diberikan.- Sebagai contoh:
- Jumlah mol = 0,75 mol NaCl
- Volume = 4,2 L.
- Sebagai contoh:
Bagilah jumlah mol dengan volume. Hasil pembagian mol berdasarkan volume adalah jumlah mol per liter larutan, atau konsentrasi molar larutan itu.
- Contoh: konsentrasi molar = jumlah mol zat terlarut / jumlah liter larutan = 0,75 mol / 4,2 L = 0,17857142

Rekam hasil Anda. Bulatkan menjadi dua atau tiga angka setelah koma, tergantung permintaan guru atau tugasnya. Saat merekam hasil Anda, singkat "konsentrasi molar" dengan "M" dan sertakan simbol kimia zat terlarut.- Sebagai contoh: 0,179 M NaCl
Metode 2 dari 4: Hitung Konsentrasi Mol dari Massa dan Volume
Perlu diketahui rumus dasar untuk menghitung konsentrasi molar. Konsentrasi molar menunjukkan hubungan antara jumlah mol zat terlarut dan volume larutan. Rumus konsentrasi molar adalah sebagai berikut: konsentrasi molar = konsentrasi zat terlarut / jumlah liter larutan
- Contoh soal: Hitung jumlah mol larutan setelah melarutkan 3,4 g KMnO4 dalam 5,2 liter air.

Analisis topiknya: Untuk mengetahui konsentrasi molar, Anda membutuhkan jumlah mol dan volume larutan dalam liter. Jika nilai ini tidak diberikan, tetapi Anda mengetahui volume dan massa larutannya, Anda dapat menentukan jumlah mol zat terlarut sebelum menghitung konsentrasi molar.- Sebagai contoh:
- Berat = 3,4 g KMnO4
- Volume = 5,2 L
- Sebagai contoh:
Hitung massa molekul zat terlarut. Untuk menghitung jumlah mol zat terlarut dari massa atau gram zat terlarut tersebut, Anda harus terlebih dahulu menentukan massa molekul zat terlarut. Molekul massa zat terlarut dapat ditentukan dengan menjumlahkan atom massa setiap elemen dalam larutan. Untuk mencari atom kubik setiap unsur, gunakan tabel periodik unsur.
- Sebagai contoh:
- Atom massa K = 39,1 g
- Atom massa Mn = 54,9 g
- Atom massa O = 16,0 g
- Jumlah atom massa = K + Mn + O + O + O + O = 39,1 + 54,9 + 16 + 16 + 16 + 16 = 158.0 g
- Sebagai contoh:
Ubah gram menjadi mol. Setelah Anda memiliki molekul kubik, Anda perlu mengalikan jumlah gram zat terlarut dalam larutan dengan faktor konversi 1 mol per massa molar zat terlarut. Hasil perkalian ini adalah banyaknya mol zat terlarut.
- Contoh: gram zat terlarut * (1 / massa molar zat terlarut) = 3,4 g * (1 mol / 158 g) = 0,0215 mol
Bagilah jumlah mol dengan banyaknya liter. Sekarang setelah Anda menghitung jumlah mol, sekarang bagi angka tersebut dengan volume larutan dalam liter, Anda akan mendapatkan konsentrasi molar dari larutan tersebut.
- Contoh: konsentrasi molar = jumlah mol zat terlarut / jumlah liter larutan = 0,0215 mol / 5,2 L = 0,004134615
Rekam hasil Anda. Anda perlu membulatkan hasil seperti yang diminta oleh guru, biasanya dua hingga tiga angka setelah koma. Selain itu, saat menulis hasil, singkatnya "konsentrasi molar" sebagai "M" dan menyertai simbol kimia zat terlarut.
- Sebagai contoh: 0,004 M KMnO4
Metode 3 dari 4: Hitung konsentrasi Molar dari Jumlah mol dan Mililiter larutan
Perlu mengetahui rumus konsentrasi molar. Untuk menghitung konsentrasi molar. Anda perlu menghitung jumlah mol zat terlarut per liter larutan, bukan mililiter larutannya. Rumus umum untuk menghitung konsentrasi molar adalah: konsentrasi molar = jumlah mol zat terlarut / jumlah liter larutan
- Contoh: Hitung konsentrasi molar dari larutan yang mengandung 1,2 mol CaCl2 dalam 2905 mililiter air.
Analisis topiknya. Untuk menghitung konsentrasi molar, Anda membutuhkan jumlah mol zat terlarut dan volume larutan dalam liter. Jika volume solusi diberikan dalam soal dalam mililiter, konversikan ke volume ekuivalen dalam liter sebelum melakukan perhitungan.
- Sebagai contoh:
- Jumlah mol = 1,2 mol CaCl2
- Volume = 2905 ml
- Sebagai contoh:
Ubah mililiter menjadi liter. Untuk mengubah larutan dari mililiter ke liter, bagilah angka dalam mililiter dengan 1000, karena setiap liter sama dengan 1000 mililiter. Anda juga dapat mengonversi mililiter ke liter dengan menggeser koma desimal 3 digit ke kiri.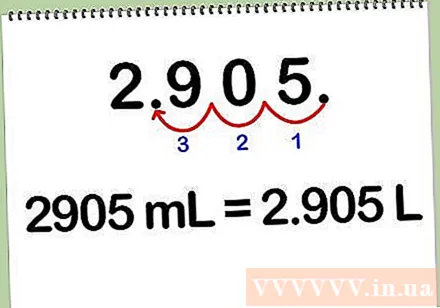
- Contoh: 2905 ml * (1 L / 1000 ml) = 2.905 L
Bagilah jumlah mol dengan banyaknya liter. Setelah mengetahui banyaknya liter, Anda dapat menghitung konsentrasi molar dengan membagi jumlah mol dengan banyaknya liter larutan.
- Contoh: konsentrasi molar = jumlah mol zat terlarut / jumlah liter larutan = 1,2 mol CaCl2 / 2.905 L = 0,413080895
Rekam hasil Anda. Ingatlah untuk membulatkan hasil menjadi dua atau tiga koma, atau seperti yang diminta oleh guru Anda. Saat mencatat hasil, singkatnya "konsentrasi molar" sebagai "M" dan kemudian simbol kimia untuk zat terlarut.
- Sebagai contoh: 0,413 M CaCl2
Metode 4 dari 4: Latihan Ekstra
Hitung konsentrasi molar suatu larutan ketika 5,2 g NaCl dilarutkan dalam 800 ml air. Tentukan nilai yang diberikan oleh soal: massa dalam gram dan volume dalam mililiter.
- Massa = 5,2 g NaCl
- Volume = 800 ml air
Temukan molekul massa NaCl dengan menjumlahkan atom kubik unsur Na, dan atom kubik Cl.
- Atom massa Na = 22,99 g
- Atom massa Cl = 35,45 g
- Molekul massa NaCl = 22,99 + 35,45 = 58,44 g
Kalikan massa zat terlarut dengan faktor konversi molar. Dalam contoh ini, massa molekul NaCl adalah 58,44 g, jadi faktor konversinya adalah “1 mol / 58,44 g”.
- Jumlah mol NaCl = 5,2 g NaCl * (1 mol / 58,44 g) = 0,8898 mol = 0,09 mol
Bagilah 800 ml air dengan 1000, Anda akan mendapatkan volume air dalam liter.
- Anda juga bisa mengalikan 800 ml dengan faktor konversi 1 L / 1000 ml dari mililiter ke liter.
- Untuk mempersingkat proses perkalian seperti di atas, Anda dapat memundurkan koma desimal 3 digit ke kiri.
- Volume = 800 ml * (1 L / 1000 ml) = 800 ml / 1000 ml = 0,8 L
Bagilah jumlah mol zat terlarut dengan volume larutan dalam liter. Untuk menghitung konsentrasi molar, Anda perlu membagi 0,09 mol zat terlarut (dalam hal ini, NaCl) dengan volume larutan dalam liter.
- Konsentrasi molar = jumlah mol zat terlarut / jumlah liter larutan = 0,09 mol / 0,8 L = 0,1125 mol / L
Catat hasil akhirnya. Bulatkan hasilnya menjadi dua atau tiga angka setelah koma dan singkatkan "konsentrasi molar" dengan "M" bersama dengan simbol kimia zat terlarut.
- Hasil: 0,11 M NaCl